У травні 2025 року Управління з контролю за продуктами і ліками США (FDA) вперше схвалило генну терапію для лікування рідкісного офтальмологічного захворювання — макулярної телангіектазії типу 2 (MacTel типу 2). Це рішення стало історичним кроком у напрямку боротьби з прогресуючими формами втрати зору, які раніше вважалися невиліковними.
Схвалення відкриває нову еру в офтальмології, особливо для людей старшого віку, які стикаються з віковими захворюваннями очей. Подія стосується не лише пацієнтів у США, а й мільйонів людей по всьому світу, включно з Україною, де проблема вікової втрати зору набуває все більшої актуальності через старіння населення.
Що таке макулярна телангіектазія типу 2?
Макулярна телангіектазія типу 2 — це прогресуюче нейродегенеративне захворювання сітківки, що характеризується патологічною перебудовою кровоносних судин у макулі — центральній ділянці сітківки, відповідальній за чітке бачення.
Хвороба зазвичай проявляється в середньому віці (переважно після 40 років) і має повільний, але невпинний перебіг. Пацієнти скаржаться на розмитість зору, спотворення прямих ліній (метаморфопсія), труднощі при читанні або розпізнаванні облич. У міру прогресування хвороба призводить до значного зниження якості життя.
Патогенез пов’язаний зі зниженням рівня серинового метаболізму та функціональними порушеннями гліальних клітин сітківки. До цього часу не існувало затверджених терапевтичних рішень, які б зупиняли або сповільнювали процес.
Проривна генна терапія: RGX-314-M
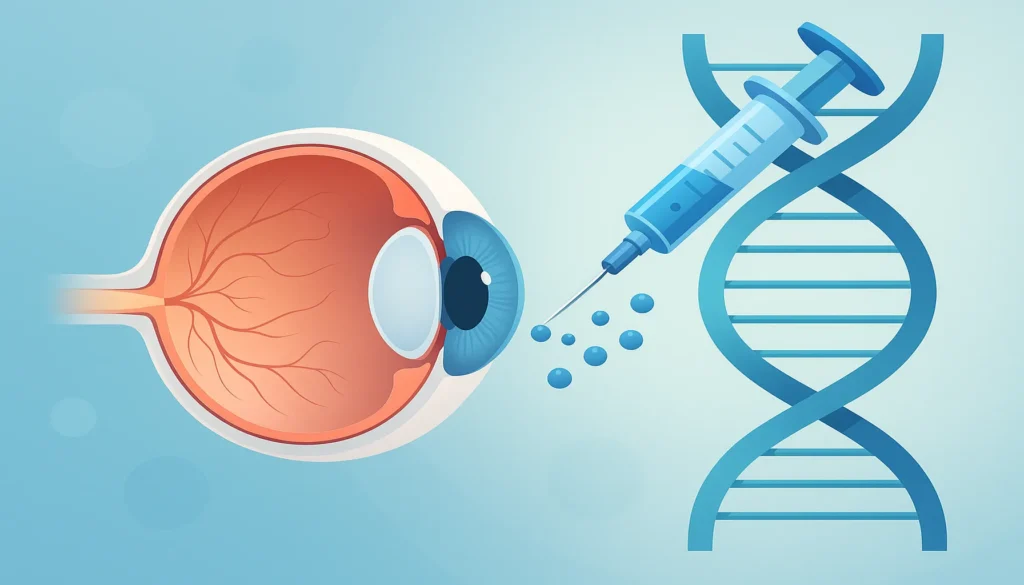
У відповідь на медичний виклик компанія RegenXBio розробила препарат RGX-314-M — генну терапію на основі аденоасоційованого вірусу (AAV8). Цей вірус використовується як вектор для доставки гена, що кодує анти-VEGF білок, безпосередньо в клітини сітківки. Після одноразової ін’єкції клітини самостійно починають виробляти терапевтичний білок, який запобігає розростанню патологічних судин та прогресуванню хвороби.
Під час міжнародного мультицентрового клінічного дослідження фази 2/3 у 2023–2024 роках понад 120 пацієнтів отримали терапію. У 67% з них вдалося досягти стабілізації гостроти зору протягом 12 місяців, а у 29% — спостерігалось покращення щонайменше на 10 букв за шкалою ETDRS.
Крім того, терапія дозволила уникнути необхідності щомісячних інʼєкцій анти-VEGF препаратів, що є серйозним полегшенням для пацієнтів і значною економією у довгостроковій перспективі.
Реакція експертів та медичної спільноти
За словами докторки Емілі Чан, провідної офтальмологині Гарвардської медичної школи:
“Це безумовно найбільше досягнення в лікуванні MacTel за останні два десятиліття. Технологія дозволяє модифікувати клітинну активність на генному рівні, забезпечуючи стабільний ефект без необхідності повторного лікування.”
Водночас частина експертів наголошує на необхідності подальшого моніторингу. Професор Браян Сміт з Каліфорнійського університету висловив обережний оптимізм:
“Ми маємо слідкувати за довготривалими ефектами, щоб оцінити, чи збережеться терапевтична дія через 3–5 років, а також виключити можливі побічні реакції.”
Фінансова доступність та перспективи
Очікувана вартість терапії складе від $410 000 до $435 000 за один курс лікування. Проте виробник заявив про створення фонду доступу для малозабезпечених пацієнтів та переговори з державними страховими агентствами для покриття витрат.
В Європейському Союзі подано запит на умовну реєстрацію препарату, і перші країни, які можуть отримати доступ — Німеччина, Франція та Велика Британія. Українські офтальмологи вже коментують можливість участі в майбутніх клінічних програмах доступу.
Технологія та майбутнє генної офтальмології
Схвалення RGX-314-M — це також підтвердження швидкого розвитку технологій у галузі молекулярної офтальмології. Генна терапія вже довела ефективність у лікуванні спадкової амаврозії Лебера, а також деяких форм пігментного ретиніту. Наступними потенційними цілями для генної терапії є вікова макулярна дегенерація (ВМД) та діабетична ретинопатія.
Висновок
Схвалення FDA генної терапії RGX-314-M для лікування макулярної телангіектазії типу 2 є важливим проривом у галузі офтальмології та персоналізованої медицини. Воно відкриває нові можливості для пацієнтів, які раніше не мали ефективного лікування.
Очікується, що в найближчі роки генна терапія стане стандартом для ряду очних захворювань. Однак важливо забезпечити рівний доступ до інновацій — як у США, так і в Україні. Суспільство повинне бути готовим до етичних, фінансових і клінічних викликів, які несе нова епоха медицини.